Metalle
 Materie
Materie  Chemische ElementeMetalle sind eine Gruppe chemischer Elemente, die links im Periodensystem angeordnet sind. Bekannte Beispiele sind Gold, Silber, Platin, Natrium, Kalium, Calcium, Eisen, Kupfer und Nickel. Metalle zeichnen sich durch ihre Festigkeit, Beständigkeit und Formbarkeit aus. Metallsalze sind für den Körper als Mineralstoffe und Spurenelemente essenziell und werden auch als Arznei- und Nahrungsergänzungsmittel verabreicht.Definition
Chemische ElementeMetalle sind eine Gruppe chemischer Elemente, die links im Periodensystem angeordnet sind. Bekannte Beispiele sind Gold, Silber, Platin, Natrium, Kalium, Calcium, Eisen, Kupfer und Nickel. Metalle zeichnen sich durch ihre Festigkeit, Beständigkeit und Formbarkeit aus. Metallsalze sind für den Körper als Mineralstoffe und Spurenelemente essenziell und werden auch als Arznei- und Nahrungsergänzungsmittel verabreicht.DefinitionMetalle sind eine Gruppe chemischer Elemente, die sich, mit Ausnahme von Wasserstoff, links im Periodensystem befinden. Sie stellen die grösste Gruppe der Elemente dar. Die zwei weiteren Hauptgruppen sind die Halbmetalle und die Nichtmetalle. Zu den Nichtmetallen gehören zum Beispiel Kohlenstoff, Stickstoff, Sauerstoff, Phosphor und Schwefel. Zwei Beispiele für Halbmetalle sind Silicium und Bor.
Der menschliche Körper enthält eine Reihe essenzieller Metallsalze als Mineralstoffe und Spurenelemente, zum Beispiel Calcium, Eisen, Natrium und Kalium. Elementare Metalle werden fast ausschliesslich in der menschlichen Zivilisation zum Beispiel für Werkzeuge, Schmuck, als Baumaterial und für Elektronik genutzt. Als erstes Metall wurde in der Menschheitsgeschichte das Kupfer verwendet. Auch der sogenannte Ötzi, der vor über 5200 Jahren verstorbene „Mann aus dem Eis“, trug ein Kupferbeil bei sich.
Kupferdraht, zum Vergrössern anklicken. Foto © PharmaWiki
Eisenoxid in Locarno, zum Vergrössern anklicken. Foto © PharmaWiki
EigenschaftenIm Folgenden sind allgemeine Eigenschaften der Metalle dargestellt. Es muss beachtet werden, dass es sich um eine grosse Gruppe chemischer Elemente mit einer entsprechenden Variabilität handelt.
Metalle zeichnen sich durch ihre Festigkeit, Beständigkeit und Formbarkeit aus. Sie haben eine glänzende und reflektierende Oberfläche und sie sind gute elektrische und thermische Leiter. Metalle lassen sich gut bearbeiten, dehnen, walzen und zu einem Draht formen. Dies im Unterschied zu Salzen und Nichtmetallen, die brüchig sind.
Metalle haben eine hohe Dichte und in der Regel einen hohen Schmelzpunkt. Mit der Ausnahme von Quecksilber sind es beim Raumtemperatur Festkörper und sie sind undurchsichtig.
Weil viele Metalle aufgrund der Valenzelektronen als Reduktionsmittel aktiv sind, kommen reine Metalle in der Natur selten vor. Ausnahmen sind Gold, Palladium und Platin, die an der Luft nicht oxidieren und wenig reaktiv sind.
Nur zwei Metalle sind farbig, nämlich Gold und Kupfer. Mit Ausnahme von Kalium und Natrium sind Metalle hart. Und Metalle kommen elementar oder in Form von Legierungen vor, d.h. als Mischungen von Metallen mit anderen Metallen oder Elementen. Mit Legierungen können die Eigenschaften der Metalle für den praktischen Gebrauch verbessert werden. Bekannte Legierungen sind zum Beispiel Stahl, rostfreier Stahl, Bronze und Messing.
Nur drei Metalle sind magnetisch, nämlich Eisen, Cobalt und Nickel.
Viele dieser Eigenschaften beruhen auf der metallischen Bindung in den Stoffen. Die Atome liegen in Metallen geordnet in einem Gitter vor. Die äusserten Elektronen koppeln sich vom Atom ab und bewegen sich frei innerhalb dieses Gitters. Das wird als Elektronenwolke bezeichnet und ist die Ursache für die gute elektrische und thermische Leitfähigkeit.
Metalle kommen in der Natur einerseits gediegen vor, sie werden aber grösstenteils aus Mineralien und Gesteinen gewonnen. Das Schmelzen und Versetzen mit Kohle ist eine traditionelle Variante. Dabei wird der Sauerstoff vom Kohlenstoff gebunden und entweicht als Kohlenstoffdioxid (CO2).
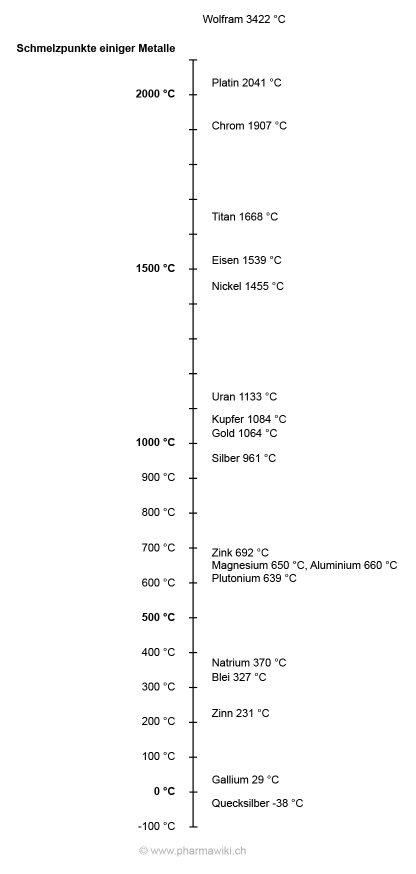
Schmelzpunkte wichtiger Metalle, zum Vergrössern anklicken. Illustration © PharmaWiki
VertreterEinige Beispiele von Metallen:
- Silber (Ag)
- Gold (Au)
- Eisen (Fe)
- Chrom (Cr)
- Natrium (Na)
- Platin (Pt)
- Blei (Pb)
- Zinn (Sn)
- Zink (Zn)
- Quecksilber (Hg)
- Nickel (Ni)
- Kupfer (Cu)
- Calcium (Ca)
- Magnesium (Mg)
- Titan (Ti)
Metalle werden zum Beispiel in Alkalimetalle, Erdalkalimetalle, Leichtmetalle, Schwermetalle, unedle Metalle und Edelmetalle eingeteilt.
ReaktionenMetalle sind in der Regel Reduktionsmittel. Zusammen mit einem Oxidationsmittel entstehen Metalloxide:
- 2 Mg (Magnesium) + O2 (Sauerstoff) → 2 MgO (Magnesiumoxid)
Die Metalloxide haben basische Eigenschaften. Mit Wasser bildet sich aus Magnesiumoxid das Magnesiumhydroxid:
- MgO (Magnesiumoxid) + H2O (Wasser) → Mg(OH)2 (Magnesiumhydroxid)
Eine Auswahl pharmazeutischer Anwendungsgebiete:
- Metallsalze werden als Arzneimittel verwendet, zum Beispiel Calcium, Magnesium, Eisen oder Lithium.
- Als Nahrungsergänzungsmittel.
- Als Desinfektionsmittel, z.B. Silber.
- Kupfer als Verhütungsmittel.
- Als Reagenzien, Katalysatoren und Chemikalien.
Metalle können eine Metallallergie verursachen (siehe dort).
siehe auchMetallallergie, Materie, Nichtmetalle, Halbmetalle, Elektrischer Strom, Mineralien, Rohstoffe
Literatur- Arzneimittel-Fachinformation (CH)
- Europäisches Arzneibuch PhEur
- Fachliteratur
- Lehrbücher der Chemie und Mineralogie
Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.