Natrium
 Arzneimittelgruppen
Arzneimittelgruppen  Chemische Elemente
Chemische Elemente  Alkalimetalle
Alkalimetalle  MineralstoffeNatrium (Na) ist ein chemisches Element, das als weiches und leichtes Alkalimetall mit einer hohen Reaktivität vorliegt. Es kommt in der Natur nicht elementar, sondern hauptsächlich als Natriumion in Form von Salzen und in Mineralien vor. Im menschlichen Körper ist Natrium als essenzieller Mineralstoff unter anderem an der Regulation des Flüssigkeitshaushalts, der Muskel- und Nervenfunktion, der normalen Zellfunktion und bei der Aufnahme von Nährstoffen beteiligt. Es ist in zahlreichen Salzen enthalten, die in der Pharmazie als Wirk- und Hilfsstoffe verwendet werden. Ein übermässiger Konsum, hauptsächlich in Form von Kochsalz, wird mit negativen gesundheitlichen Folgen in Verbindung gebracht.Produkte
MineralstoffeNatrium (Na) ist ein chemisches Element, das als weiches und leichtes Alkalimetall mit einer hohen Reaktivität vorliegt. Es kommt in der Natur nicht elementar, sondern hauptsächlich als Natriumion in Form von Salzen und in Mineralien vor. Im menschlichen Körper ist Natrium als essenzieller Mineralstoff unter anderem an der Regulation des Flüssigkeitshaushalts, der Muskel- und Nervenfunktion, der normalen Zellfunktion und bei der Aufnahme von Nährstoffen beteiligt. Es ist in zahlreichen Salzen enthalten, die in der Pharmazie als Wirk- und Hilfsstoffe verwendet werden. Ein übermässiger Konsum, hauptsächlich in Form von Kochsalz, wird mit negativen gesundheitlichen Folgen in Verbindung gebracht.ProdukteNatrium ist in zahlreichen Arzneimitteln in Wirk- und Hilfsstoffen enthalten. Im Englischen wird es als Sodium bezeichnet, aber wie im Deutschen mit Na abgekürzt.
Struktur und EigenschaftenNatrium (Na, Atommasse: 22.989 g/mol) ist ein chemisches Element aus der Gruppe der Alkalimetalle mit der Ordnungszahl 11. Es liegt elementar als weiches, silbernes Metall vor, das sehr reaktiv ist und deshalb in Mineralöl (Paraffinen) aufbewahrt wird. Es oxidiert an der Luft rasch und wird grau. Das Metall hat eine leicht geringere Dichte als Wasser und kann mit einem Messer geschnitten werden. Natrium hat einen tiefen Schmelzpunkt von 98 °C.
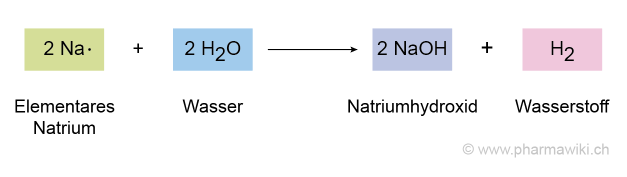
Natrium gibt sein Valenzelektron gerne ab und ist deshalb sehr reaktiv. Aus diesem Grund kommt es auch in der Natur nicht elementar vor. Wird es zum Beispiel mit Wasser in Verbindung gebracht, reagiert es heftig unter einer exothermen Reaktion und kann sogar explodieren:
- 2 Na (Natrium) + 2 H2O (Wasser) → 2 NaOH (Natriumhydroxid) + H2 (Wasserstoff)
Dabei handelt es sich um eine → Redox-Reaktion.
Die heftige Reaktion von Natrium mit Wasser, zum Vergrössern anklicken. Illustration © PharmaWiki
Natrium gehört zu den Elementen, die am häufigsten auf der Erde vorkommen, nicht nur im Meerwasser und in Salzminen, sondern auch im Gestein wie dem Feldspat.
In Arzneimitteln ist es ausschliesslich als Natriumion (Na+) in Form von Salzen enthalten, von denen zahlreiche existieren, zum Beispiel Natriumchlorid (Kochsalz, NaCl), Natriumsulfat (Glaubersalz), Natriumhydrogencarbonat (Natron), Natriumcarbonat (Soda) oder Natriumhydroxid (NaOH). Zahlreiche Wirkstoffe liegen als Natriumsalze vor.
Natriumchlorid, zum Vergrössern anklicken. Foto © PharmaWiki
WirkungenNatrium nimmt im menschlichen Körper lebenswichtige Funktionen wahr. Es ist zum Beispiel an der Regulation des Blutdrucks, des Flüssigkeitshaushalts, der Muskel- und Nervenfunktion, der normalen Zellfunktion und bei der Aufnahme von Nährstoffen beteiligt. Die Zufuhr erfolgt über die Ernährung und die Ausscheidung hauptsächlich über die Nieren mit dem Harn.
Die Konzentration von Natriumionen in den Zellen ist wesentlich geringer als ihre extrazelluläre Konzentration. Aufrecht erhalten wird der Unterschied (Gradient) von der Na+/K+-ATPase, einem primär aktiven Transporter unter dem Verbrauch von ATP.
Die unterschiedlichen Ionenkonzentrationen und ihre Veränderungen sind die Basis für die Entstehung von Ruhemembran- und Aktionspotentialen und die Leitung von Impulsen in Nervenzellen. Zu Beginn des Aktionspotentials strömt Natrium durch spannungsabhängige Natriumkanäle in die Zelle ein und führt zu einer Depolarisation. Auch an der Reizleitung am Herzen ist Natrium entsprechend beteiligt.
AnwendungsgebieteIn der Pharmazie:
- Natrium ist in zahlreichen Wirkstoffsalzen enthalten, unter anderem zur Erhöhung der Wasserlöslichkeit.
- Viele pharmazeutische Hilfsstoffe enthalten Natrium.
- Zahlreiche Anwendungsgebiete als → Natriumchlorid (siehe dort).
- Für Radiopharmaka (Isotope).
Natrium ist ein essenzieller Mineralstoff, der mit der Nahrung täglich aufgenommen wird.
Unerwünschte WirkungenEine übermässige Zufuhr von Natrium – meist in Form von Kochsalz (Natriumchlorid) – wird mit negativen gesundheitlichen Folgen in Verbindung gebracht, insbesondere mit Bluthochdruck und Herz-Kreislauf-Erkrankungen. Deshalb wird im Allgemeinen eine Reduktion unseres übermässigen Salzkonsums empfohlen.
siehe auchNatriumchlorid, Metalle, Alkalimetalle
Literatur- American Heart Association (AHA)
- Arzneimittel-Fachinformation (CH)
- Bundesinstitut für Risikobewertung (BfR)
- European Medicines Agency (EMA)
- Europäisches Arzneibuch PhEur
- He F.J., MacGregor G.A. A comprehensive review on salt and health and current experience of worldwide salt reduction programmes. J Hum Hypertens, 2009, 23(6), 363-84 Pubmed

- International Union of Pure and Applied Chemistry (IUPAC)
- Kotchen T.A., Cowley A.W. Jr., Frohlich E.D. Salt in health and disease--a delicate balance. N Engl J Med, 2013, 368(13), 1229-37 Pubmed

- Lehrbücher der Chemie
- World Health Organization (WHO)
Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.