Calciumcarbonat
 Arzneimittelgruppen
Arzneimittelgruppen  Salze
Salze  Antazida / Phosphatbinder / BasenCalciumcarbonat ist ein Wirkstoff aus der Gruppe der Calciumsalze, der in der Natur unter anderem im Kalkstein, in Muschelschalen und Perlen vorkommt. Calciumcarbonat wird medizinisch bei Magenbrennen und saurem Aufstossen, als Phosphatbinder bei erhöhten Phosphatwerten sowie als Quelle für Calcium für die Vorbeugung und Behandlung eines Calciummangels und einer Osteoporose verabreicht. Die Dosis ist abhängig vom Produkt und Anwendungsgebiet. Zu den möglichen unerwünschten Wirkungen gehören gastrointestinale Störungen. Calciumcarbonat soll nicht überdosiert werden, weil daraus eine potenziell gefährliche Hyperkalzämie entstehen kann. Es kann Arzneimittel-Wechselwirkungen verursachen.
Antazida / Phosphatbinder / BasenCalciumcarbonat ist ein Wirkstoff aus der Gruppe der Calciumsalze, der in der Natur unter anderem im Kalkstein, in Muschelschalen und Perlen vorkommt. Calciumcarbonat wird medizinisch bei Magenbrennen und saurem Aufstossen, als Phosphatbinder bei erhöhten Phosphatwerten sowie als Quelle für Calcium für die Vorbeugung und Behandlung eines Calciummangels und einer Osteoporose verabreicht. Die Dosis ist abhängig vom Produkt und Anwendungsgebiet. Zu den möglichen unerwünschten Wirkungen gehören gastrointestinale Störungen. Calciumcarbonat soll nicht überdosiert werden, weil daraus eine potenziell gefährliche Hyperkalzämie entstehen kann. Es kann Arzneimittel-Wechselwirkungen verursachen. synonym: Calcii carbonas PhEur, Kalk, CI 77220, E 170
ProdukteCalciumcarbonat ist als Arzneimittel unter anderem in Form von Tabletten, Kapseln, Brausetabletten, Kautabletten, Lutschtabletten, Kaugummis und als Suspension zum Einnehmen im Handel. Bei einigen Produkten handelt es sich um Kombinationspräparate, zum Beispiel mit Vitamin D3 oder anderen Antazida.
Struktur und EigenschaftenCalciumcarbonat (CaCO3, Mr = 100.1 g/mol) liegt in Arzneibuchqualität als weisses bis fast weisses Pulver vor, das in Wasser praktisch unlöslich ist. In der Natur findet es sich beispielsweise im Kalkstein (einem Sedimentgestein), in den Mineralien Calcit (Kalkspat) und Aragonit, im Marmor, in der Kreide, in Muschelschalen, Eierschalen, Schneckenhäusern und in Perlen. Calciumcarbonat wird auch als Kalk bezeichnet.
Hartes Wasser bildet sich aus Calciumcarbonat im Gestein, das mit CO2-gesättigtem Wasser in Kontakt kommt. Dabei entsteht das lösliche Calciumhydrogencarbonat (Ca(HCO3)2). Hartes Wasser kann umgekehrt zu Calciumcarbonat-Ablagerungen führen.
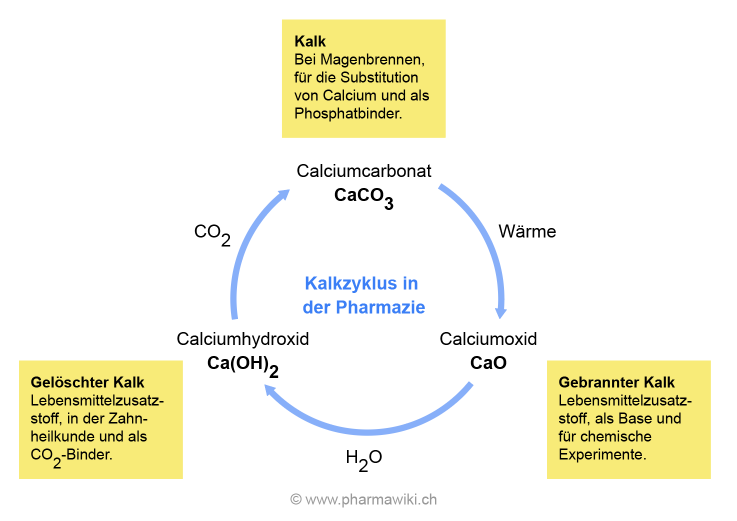
Bei der Einwirkung von Hitze entsteht aus Calciumcarbonat der gebrannte Kalk Calciumoxid, der mit Wasser in einer stark exothermen Reaktion zum gelöschten Kalk Calciumhydroxid reagiert.
Der Kalkzyklus in der Pharmazie, zum Vergrössern anklicken. Illustration © PharmaWiki
WirkungenCalciumcarbonat ist eine Base, welche die Magensäure neutralisiert. Das Carbonat wird von der Säure protoniert und bildet die Kohlensäure, welche rasch zu Kohlenstoffdioxid und Wasser zerfällt:
- 2 HCl (Salzsäure) + CaCO3 (Calciumcarbonat) → CaCl2 (Calciumchlorid) + H2O (Wasser) + CO2 (Kohlenstoffdioxid) ↑
Die Entstehung von Calciumchlorid im Magen ist auch die Grundlage für den Einsatz bei einer Hyperphosphatämie. Calciumchlorid bildet mit Phosphationen aus der Nahrung unlösliche Calciumphosphatsalze, die mit dem Stuhl ausgeschieden werden. Auf diese Weise wird die Phosphatbelastung reduziert.
Calcium gehört zu den wichtigsten Mineralstoffen und ist unter anderem für den Aufbau der Knochen und Zähne, für die Reizleitung der Nervenzellen, die Muskulatur, das Herz und die Blutgerinnung von Bedeutung.
Anwendungsgebiete- Zur Vorbeugung und Behandlung eines Calciummangels (Calciumsubstitution).
- Zur Vorbeugung und Behandlung einer Osteoporose (Calciumsubstitution).
- Für die Behandlung von Magenbrennen und saurem Aufstossen (gastroösophagaler Reflux).
- Als Phosphatbinder für die Behandlung einer Hyperphosphatämie bei einer chronischen Niereninsuffizienz bei Patienten unter einer Dialyse.
Calciumcarbonat wird auch als pharmazeutischer Hilfsstoff verwendet, beispielsweise für die Herstellung von Tabletten. Es gehört zu den Pigmenten.
DosierungGemäss der Fachinformation. Die Dosierung ist vom Produkt und vom Anwendungsgebiet abhängig. Die übliche Tagesdosis liegt für Erwachsene im Bereich von 500 bis 1500 mg Calcium. Antazida sollen nicht überdosiert werden.
KontraindikationenZu den Gegenanzeigen gehören (Auswahl):
- Überempfindlichkeit
- Erhöhte Calciumwerte (Hyperkalzämie)
- Nierensteine
- Kinder und Jugendliche (abhängig vom Präparat)
Die vollständigen Vorsichtsmassnahmen finden sich in der Arzneimittel-Fachinformation.
InteraktionenCalcium kann die Absorption anderer Medikamente hemmen. Dies gilt zum Beispiel für bestimmte Antibiotika wie die Tetrazykline und die Chinolone sowie für Eisen, Levothyroxin und Bisphosphonate. Ein ausreichender zeitlicher Abstand von mindestens zwei bis drei Stunden muss eingehalten werden. Calcium kann ferner die Effekte der Herzglykoside verstärken und die Oxalsäure kann die Calciumaufname verringern. Weitere Interaktionen wurden beschrieben, zum Beispiel mit Thiaziden und Vitamin D.
Unerwünschte WirkungenWeil sich beim Kontakt mit der Magensäure das Gas Kohlenstoffdioxid bildet, kann Calciumcarbonat zu einem geblähten Magen und Aufstossen führen. Weitere möglichen unerwünschte Wirkungen sind eine Verstopfung, Flatulenz, Übelkeit, Bauchschmerzen, Durchfall und eine reaktive Magensäuresekretion (Acid Rebound). Eine Überdosierung kann zu einer potenziell gefährlichen Hyperkalzämie führen.
siehe auchCalcium, Antazida, Phosphatbinder, Basen, Calciumoxid, Calciumhydroxid, Hartes Wasser, Muscheln
Literatur- Al Omari M.M., Rashid I.S., Qinna N.A., Jaber A.M., Badwan A.A. Calcium Carbonate. Profiles Drug Subst Excip Relat Methodol, 2016, 41, 31-132 Pubmed

- Arzneimittel-Fachinformation (CH, D, USA, UK)
- Europäisches Arzneibuch PhEur
- Lehr- und Handbücher der Chemie
- Makoff R. The value of calcium carbonate in treating acidosis, phosphate retention, and hypocalcemia. Nephrol News Issues, 1991, 5(7), 16, 18-9, 32 Pubmed

Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.
Weitere Informationen