Calciumoxid
 PharmaWikiCalciumoxid ist das basische Oxid von Calcium. Es kann aus Calciumcarbonat (Kalk, Kalkstein) durch Erhitzen gewonnen werden. Calciumoxid reagiert mit Wasser in einer stark exothermen Reaktion zur Calciumhydroxid. Es hat ätzende, reizende und basische Eigenschaften und muss deshalb unter Beachtung der Vorsichtsmassnahmen gehandhabt werden. Calciumoxid wird unter anderem als Lebensmittelzusatzstoff, als Base und für chemische Experimente verwendet.
PharmaWikiCalciumoxid ist das basische Oxid von Calcium. Es kann aus Calciumcarbonat (Kalk, Kalkstein) durch Erhitzen gewonnen werden. Calciumoxid reagiert mit Wasser in einer stark exothermen Reaktion zur Calciumhydroxid. Es hat ätzende, reizende und basische Eigenschaften und muss deshalb unter Beachtung der Vorsichtsmassnahmen gehandhabt werden. Calciumoxid wird unter anderem als Lebensmittelzusatzstoff, als Base und für chemische Experimente verwendet. synonym: Calcii oxidum, CaO, Gebrannter Kalk, Calcium oxide, E 529
ProdukteCalciumoxid ist als Reinstoff in Apotheken und Drogerien erhältlich.
Struktur und EigenschaftenCalciumoxid (CaO, Mr = 56.08 g/mol) ist das basische Oxid von Calcium. Es liegt als weisses und geruchloses Pulver vor und reagiert stark mit Wasser (siehe unten). Es soll deshalb vor Feuchtigkeit geschützt gelagert werden.
Es kann zum Beispiel aus Calciumcarbonat (Kalk) resp. aus Kalkstein durch Erhitzen bei über 825°C gewonnen werden.
- CaCO3 (Calciumcarbonat) → CaO (Calciumoxid) + CO2 (Kohlenstoffdioxid)
Aufgrund der Herstellung mit Wärme wird Calciumoxid auch als gebrannter Kalk bezeichnet. Calciumhydroxid, das mit Wasser aus Calciumoxid hergestellt wird, heisst gelöschter Kalk.
Bei der Zugabe von Wasser entsteht Calciumhydroxid. Diese Reaktion verläuft stark exotherm:
- CaO (Calciumoxid) + H2O (Wasser) → Ca(OH)2 (Calciumhydroxid) + Energie (Wärme)
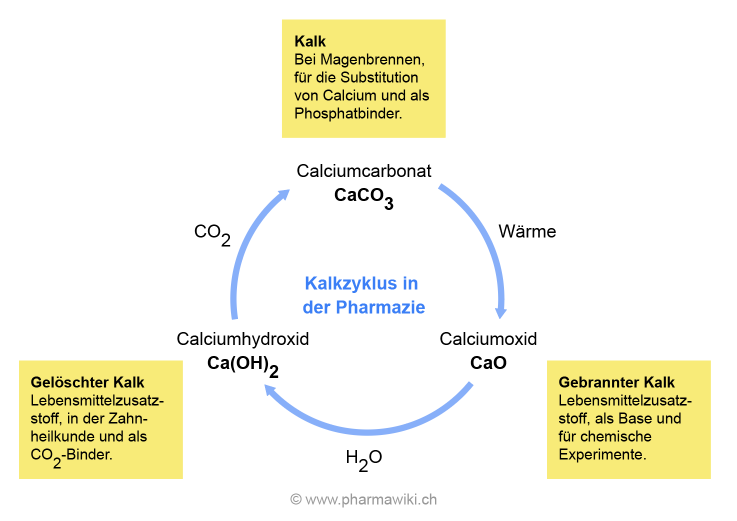
Der Kalkzyklus in der Pharmazie, zum Vergrössern anklicken. Illustration © PharmaWiki
WirkungenCalciumoxid hat stark ätzende, reizende, basische und antiseptische Eigenschaften.
AnwendungsgebieteZu den Anwendungsgebieten gehören (Auswahl):
- Als Lebensmittelzusatzstoff, unter anderem als Säureregulator (E 529).
- Als Base.
- Für die Herstellung von Calciumhydroxid.
- Für chemische Experimente: Herstellung aus Calciumcarbonat, Reaktion mit Wasser, Drummondsches Licht bei starkem Erhitzen, Bindung von Kohlenstoffdioxid mit Calciumhydroxid.
Calciumoxid kann bei einer unsachgemässen Handhabung zu schweren Reizungen der Haut, der Atemwege und zu schweren Augenreizungen und -schädigungen führen. Die entsprechenden Vorsichtsmassnahmen im Sicherheitsdatenblatt müssen deshalb beachtet werden (z.B. das Tragen einer Schutzbrille, von Schutzkleidung und Handschuhen).
siehe auchCalciumhydroxid, Calciumcarbonat
Literatur- Arzneimittel-Fachinformation (CH)
- Europäisches Arzneibuch PhEur
- Fachliteratur
- Lehrbücher der Chemie
- Lexika der Pharmazie
- Royal Society of Chemistry (RSC)
- Sicherheitsdatenblatt
Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.
Weitere Informationen