Salpetersäure
 SäurenDie Salpetersäure (HNO3) ist eine starke Säure mit ätzenden, auflösenden und oxidierenden Eigenschaften.
SäurenDie Salpetersäure (HNO3) ist eine starke Säure mit ätzenden, auflösenden und oxidierenden Eigenschaften. synonym: Acidum nitricum PhEur, Salpetergeist, HNO3, Aqua fortis, Nitric acid
ProdukteDie Salpetersäure ist in Apotheken und Drogerien in verschiedenen Konzentrationen erhältlich.
Struktur und EigenschaftenDie Salpetersäure (HNO3, Mr = 63.0 g/mol) liegt als klare bis fast farblose Flüssigkeit mit einem stechenden Geruch vor, die mit Wasser mischbar ist. Sie kann sich gelblich verfärben. Es existieren verschiedene Konzentrationen. Dazu gehören:
- Rauchende Salpetersäure: ab etwa 85 %
- Konzentrierte Salpetersäure: 69 % (68 % bis 70 %, m/m)
- Salpetersäure 65 %
- Verdünnte Salpetersäure: 25 %
Die Salpetersäure hat ätzende, lytische, korrosive, brandfördernde und oxidierende Eigenschaften. Sie gehört zu den stärksten Säuren mit einem pKa von -1.4. Sie kann jedoch auch als Base reagieren. Ihre Dichte ist grösser als diejenige von Wasser.
Die Salze der Salpetersäure werden als Nitrate (Salpeter) bezeichnet. Dazu gehören zum Beispiel Kaliumnitrat und Natriumnitrat. Sie werden unter anderem als Lebensmittelzusatzstoffe zum Konservieren von Fleisch und Wurstwaren verwendet (Pökeln). Sie lassen sich mit einer Säure-Base-Reaktion herstellen:
- HNO3 (Salpetersäure) + KOH (Kaliumhydroxid) → KNO3 (Kaliumnitrat) + H2O (Wasser)
Die Salpetersäure ist ein starkes Oxidationsmittel und oxidiert viele Metalle, jedoch nicht Gold oder Platin. Deshalb lässt sich Gold mit der Säure auf seine Echtheit prüfen. Wird die Salpetersäure jedoch mit Salzsäure gemischt, entsteht das Königswasser, mit dem sich sogar Gold lösen lässt.
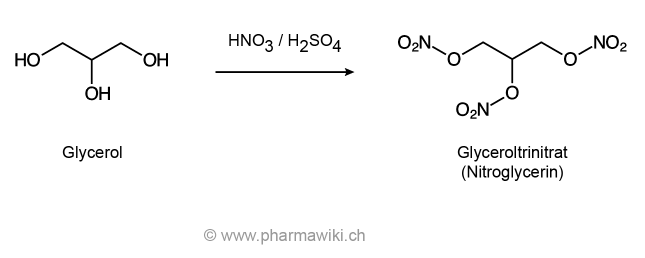
Anwendungsgebiete (Auswahl)- Für die Synthese des Wirkstoffs Nitroglycerin.
- Als Reagens.
- Für die synthetische Chemie (Nitrogruppe, Nitrierung).
- Für die Herstellung von Nitratdünger.
- Zahlreiche technische Anwendungen.
- Medizinisch für die Behandlung von Warzen (geeignete Zubereitungen!)
Salpetersäure kann zur illegalen Herstellung von Sprengstoffen missbraucht werden. Dazu wird sie mit Schwefelsäure gemischt, woraus die sogenannte Nitriersäure entsteht. Zu den Explosivstoffen, welche mit der Nitriersäure hergestellt werden, gehören die Nitrocellulose, Nitroglycerin, Pikrinsäure und TNT. Die Salpetersäure gehört zu den Vorläuferstoffen für Explosivstoffe.
Synthese von Nitroglycerin, zum Vergrössern anklicken. Illustration © PharmaWiki
Unerwünschte WirkungenDie Salpetersäure hat reizende und ätzende Eigenschaften und kann bei einer unsachgemässen Anwendung schwere Verätzungen der Haut, der Atemwege und der Augen hervorrufen. Deshalb müssen die Angaben im Sicherheitsdatenblatt genau beachtet werden. Bei der Arbeit mit Salpetersäure sollen Schutzkleidung, Handschuhe und eine Schutzbrille getragen werden. Die Dämpfe dürfen nicht eingeatmet werden.
Die Salpetersäure hat ferner oxidierende und brandfördernde Eigenschaften und soll vor brennbaren Materialien ferngehalten werden. Das Verschlucken ist lebensgefährlich.
siehe auchSchwefelsäure, Säuren, Vorläuferstoffe für Explosivstoffe
Literatur- Fachliteratur
- Lehr- und Handbücher der organischen Chemie
- Sicherheitsdatenblatt
Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.
Weitere Informationen