Fluor
 Arzneimittelgruppen
Arzneimittelgruppen  SpurenelementeFluor ist ein chemisches Element, das als toxisches und hochreaktives Gas mit einer leicht gelben Farbe und einem stechenden Geruch vorliegt. Die Salze mit dem Anion Fluorid spielen eine zentrale Rolle bei der Vorbeugung von Karies. Sie sind unter anderem in Zahnpasten, Mundspülungen und Zahngelen enthalten. Fluoride stärken den Zahnschmelz, fördern die Remineralisation, erhöhen die Säureresistenz und sind gegen die Bakterien wirksam. Zu den möglichen unerwünschten Wirkungen gehören lokale Reaktionen in der Mundhöhle. Das gasförmige Fluor ist giftig und verursacht schwere Verätzungen. Produkte
SpurenelementeFluor ist ein chemisches Element, das als toxisches und hochreaktives Gas mit einer leicht gelben Farbe und einem stechenden Geruch vorliegt. Die Salze mit dem Anion Fluorid spielen eine zentrale Rolle bei der Vorbeugung von Karies. Sie sind unter anderem in Zahnpasten, Mundspülungen und Zahngelen enthalten. Fluoride stärken den Zahnschmelz, fördern die Remineralisation, erhöhen die Säureresistenz und sind gegen die Bakterien wirksam. Zu den möglichen unerwünschten Wirkungen gehören lokale Reaktionen in der Mundhöhle. Das gasförmige Fluor ist giftig und verursacht schwere Verätzungen. ProdukteFluoride sind in vielen Zahn- und Mundpflegeprodukten enthalten. Im Handel ist auch mit Fluoriden versetztes Kochsalz erhältlich.
Struktur und EigenschaftenFluor (F, Mr = 18.99 g/mol) ist ein chemisches Element mit der Ordnungszahl 9 aus der Gruppe der Halogene, das bei Raumtemperatur als toxisches Gas mit einer leicht gelben Farbe und einem stechenden Geruch vorliegt. Wie andere Halogene ist es elementar diatomar (F2).
Fluor besitzt 7 Valenzelektronen und erreicht mit einem zusätzlichen Elektron das Oktett, also seine optimale Elektronenkonfiguration. Fluor hat von allen Elementen die höchste Elektronegativität, ist extrem reaktiv und bildet mit fast allen anderen Elementen Verbindungen. Dies mit der Ausnahme der Edelgase Helium und Neon. Es hat eine hohe Affinität für Elektronen und ist ein starkes Oxidationsmittel.
In der Natur kommt Fluor in verschiedenen Mineralien relativ häufig vor, zum Beispiel im Fluorit (Flussspat), der aus Calciumfluorid (CaF2) besteht. Das Fluorgas kann aus Calciumfluorid mithilfe von Schwefelsäure und einer Elektrolyse gewonnen werden.
Die Salze mit dem Anion Fluorid werden als Fluoride bezeichnet, zum Beispiel Natriumfluorid, Calciumfluorid, Olaflur und Dectaflur.
Fluorit im Mineralien-Museum Cristallina in Disentis, zum Vergrössern anklicken. Foto © PharmaWiki
WirkungenFluoride hemmen die Demineralisation der Zähne, fördern ihre Remineralisation, erhöhen die Säureresistenz des Zahnschmelzes und sind bakterizid gegen die Bakterien. Sie senken das Risiko für die Entstehung der Karies.
AnwendungsgebieteFluoride:
- Für die Vorbeugung und Behandlung der Karies
- Behandlung empfindlicher Zahnhälse
- Fluoridierung des Trinkwassers und des Kochsalzes
- Für Radiopharmaka (Isotope).
Im Drug Discovery und der Medikamentenentwicklung werden Wirkstoffkandidaten unter anderem deshalb fluoriert, weil dadurch der oxidative Metabolismus unterdrückt wird. Fluor macht die Verbindungen lipophiler und kann die Bioverfügbarkeit erhöhen.
Viele pharmazeutische Wirkstoffe enthalten an Kohlenstoff kovalent gebundenes Fluor, z.B. Flucytosin, Fluoxetin, Ciprofloxacin und Inhalationsanästhetika.
DosierungGemäss der Gebrauchsinformation. Die Produkte werden üblicherweise dreimal täglich angewandt, hochdosierte Zahngele auch nur einmal wöchentlich. Die Dosis ist abhängig vom Alter und vom Anwendungsgebiet.
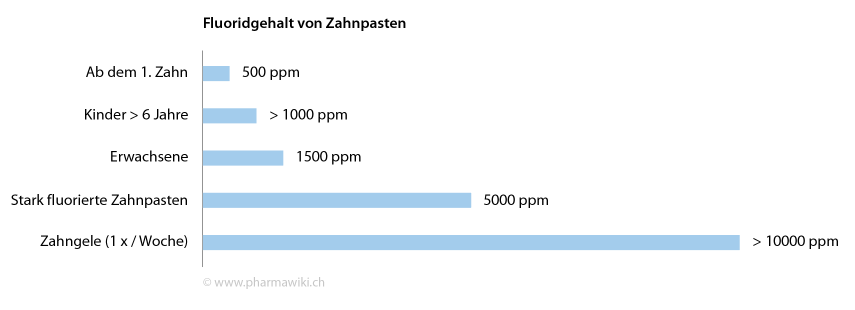
Zahnpasten unterscheiden sich in ihrem Fluoridgehalt:
- Ab dem ersten Zahn: 500 ppm
- Kinder > 6 Jahre: 1000 bis 1400 ppm
- Jugendliche und Erwachsene: 1450 bis 1500 ppm
- Zahnpasten mit hohem Fluorgehalt: 5000 ppm
- Zahngele für die wöchentliche oder monatliche Anwendung: > 10'000 bis 20'000 ppm
Fluoridgehalt von Zahnpasten, zum Vergrössern anklicken. Illustration © PharmaWiki
Kontraindikationen- Überempfindlichkeit
Die vollständigen Vorsichtsmassnahmen finden sich in der Arzneimittel-Fachinformation.
Unerwünschte WirkungenElementares Fluor ist aufgrund seiner hohen chemischen Reaktivität stark toxisch. Es wirkt brandfördernd, ist lebensgefährlich beim Einatmen und verursacht schwere Verätzungen der Atemwege, der Haut und der Augen.
Zu den möglichen unerwünschten Wirkungen der Fluoride gehören selten lokale Reaktionen in der Mundhöhle wie beispielsweise Rötungen, Brennen und Schwellungen.
Eine starke Überdosis von Fluoriden kann zu unerwünschten Wirkungen und einer Vergiftung führen. Dazu sind allerdings hohe Dosen ab 5 mg Fluor pro kg Körpergewicht erforderlich.
siehe auchLiteratur- Arzneimittel-Fachinformation (CH)
- Europäisches Arzneibuch PhEur
- Fachliteratur
- Mark A.M. Fluoride helps fight cavities. J Am Dent Assoc, 2021, 152(1), 84 Pubmed

- McGrady M.G., Ellwood R.P., Pretty I.A. Why fluoride? Dent Update, 2010, 37(9), 595-8, 601-2 Pubmed

- Rugg-Gunn A, Bánóczy J. Fluoride toothpastes and fluoride mouthrinses for home use. Acta Med Acad, 2013, 42(2),168-78 Pubmed

- Sicherheitsdatenblatt
- Toumba J. Fluoride. Eur Arch Paediatr Dent, 2009, 10(3), 127 Pubmed

Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.
Weitere Informationen