Nitroverbindungen
 StoffgruppenNitroverbindungen sind chemische Verbindungen, bei welchen eine oder mehrere Nitrogruppen (-NO2) direkt mit einem Kohlenstoffatom verbunden sind. Es wird zwischen aliphatischen und aromatischen Vertretern unterschieden. Für die Nomenklatur wird das Präfix Nitro verwendet. Nitroverbindungen sind häufig explosiv – Beispiele hierfür sind Trinitrotoluol (TNT) und die Pikrinsäure. Einige pharmazeutische Wirkstoffe sind Nitroverbindungen und werden wie beispielsweise Metronidazol und Nitrofurantoin für die Behandlung bakterieller und parasitärer Infektionskrankheiten eingesetzt. Nachteilig sind ihre mutagenen Eigenschaften.
StoffgruppenNitroverbindungen sind chemische Verbindungen, bei welchen eine oder mehrere Nitrogruppen (-NO2) direkt mit einem Kohlenstoffatom verbunden sind. Es wird zwischen aliphatischen und aromatischen Vertretern unterschieden. Für die Nomenklatur wird das Präfix Nitro verwendet. Nitroverbindungen sind häufig explosiv – Beispiele hierfür sind Trinitrotoluol (TNT) und die Pikrinsäure. Einige pharmazeutische Wirkstoffe sind Nitroverbindungen und werden wie beispielsweise Metronidazol und Nitrofurantoin für die Behandlung bakterieller und parasitärer Infektionskrankheiten eingesetzt. Nachteilig sind ihre mutagenen Eigenschaften.synonym: Nitrogruppe, NO2, Nitro, Nitro compounds
DefinitionNitroverbindungen sind chemische Verbindungen mit einer oder mehreren Nitrogruppen als funktionelle Gruppen:
R-NO2
Sie bestehen aus einem Stickstoffatom (N), an welches ein Rest -R und zwei Sauerstoffatome (O) gebunden sind.
Nitrogruppen sind direkt mit einem Kohlenstoffatom (C) verbunden. Ist R ein Sauerstoffatom (O), wird von organischen Nitraten gesprochen (-O-NO2). Nitrate sind keine Nitroverbindungen.
Nitroverbindungen werden oft mit der Salpetersäure hergestellt. Diese Reaktion wird als Nitrierung bezeichnet. Der Zusatz von Schwefelsäure kann erforderlich sein.
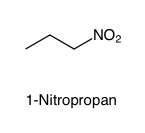
NomenklaturNitroverbindungen werden mit dem Präfix Nitro- bezeichnet. Also beispielsweise Nitromethan, 1-Nitropropan oder Nitrobenzol. Es wird zwischen aliphatischen und aromatischen Nitroverbindungen unterschieden.

Wie bei den Aminen oder Alkoholen existieren primäre, sekundäre und tertiäre Nitroverbindungen.
- Aminonitrothiazol
- Chloramphenicol
- Nitrofurantoin
- Nitrofural
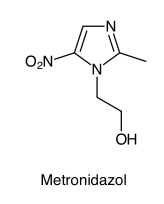
- Nitroimidazole wie Metronidazol und Ornidazol
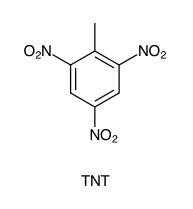
- Nitroverbindungen wie Trinitrotoluol (TNT), die Pikrinsäure und die Styphninsäure sind explosiv.
- Die Nitrogruppe hat starke elektronenziehende Eigenschaften.
- Nitroverbindungen sind polar.
- Aliphatische Nitroverbindungen können zu Aminen hydriert werden.
- Das Wasserstoffatom am Kohlenstoff in α-Position ist sauer, weil die Nitrogruppe elektronenziehende Eigenschaften hat.
Einige pharmazeutische Wirkstoffe enthalten Nitrogruppen. Sie werden unter anderem für die Behandlung parasitärer und bakterieller Infektionskrankheiten eingesetzt. Allerdings haben Nitroverbindungen mutagene Eigenschaften und finden sich deshalb vorwiegend in älteren Wirkstoffen.
Literatur- Arzneimittel-Fachinformation (CH)
- Fachliteratur
- Lehrbücher der Chemie
Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.
