Crisaborol
 Arzneimittelgruppen
Arzneimittelgruppen  Phosphodiesterase-4-HemmerCrisaborol ist ein entzündungshemmender Wirkstoff aus der Gruppe der Phosphodiesterase-4-Hemmer, der zur äusserlichen Behandlung einer atopischen Dermatitis eingesetzt wird. Die Effekte beruhen auf der Hemmung des Enzyms Phosphodiesterase-4, was zu einer zu einer Erhöhung des intrazellulären cAMP und zu einer reduzierten Bildung entzündungsfördernder Zytokine führt. Die Salbe wird morgens und abends aufgetragen. Zu den häufigsten möglichen unerwünschten Wirkungen gehören Schmerzen an der Applikationsstelle.
Phosphodiesterase-4-HemmerCrisaborol ist ein entzündungshemmender Wirkstoff aus der Gruppe der Phosphodiesterase-4-Hemmer, der zur äusserlichen Behandlung einer atopischen Dermatitis eingesetzt wird. Die Effekte beruhen auf der Hemmung des Enzyms Phosphodiesterase-4, was zu einer zu einer Erhöhung des intrazellulären cAMP und zu einer reduzierten Bildung entzündungsfördernder Zytokine führt. Die Salbe wird morgens und abends aufgetragen. Zu den häufigsten möglichen unerwünschten Wirkungen gehören Schmerzen an der Applikationsstelle. synonym: Crisaborolum, AN2728, Crisaborole
ProdukteCrisaborol wurde in den USA im Jahr 2016 als Salbe zugelassen (Eucrisa®, 2 %). In der Schweiz ist Crisaborol aktuell nicht registriert.
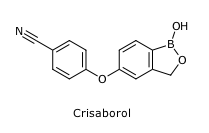
Struktur und EigenschaftenCrisaborol (C14H10BNO3, Mr = 251.0 g/mol) ist eine niedermolekulare Borverbindung mit einer nicht steroidalen Struktur. Es gehört zu den Phenoxybenzoxaborolen. Aufgrund seiner geringen Grösse kann der Wirkstoff in die oberen Hautschichten eindringen.
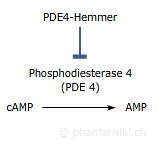
Crisaborol (ATC D11AH06  ) hat entzündungshemmende Eigenschaften. Die Effekte beruhen auf der Hemmung der Phosphodiesterase-4 (PDE-4), was zu einer zu einer Erhöhung des intrazellulären cAMP führt. Die Folge ist eine reduzierte Bildung proinflammatorischer Zytokine.
) hat entzündungshemmende Eigenschaften. Die Effekte beruhen auf der Hemmung der Phosphodiesterase-4 (PDE-4), was zu einer zu einer Erhöhung des intrazellulären cAMP führt. Die Folge ist eine reduzierte Bildung proinflammatorischer Zytokine.
Für die Behandlung der atopischen Dermatitis (Neurodermitis).
DosierungGemäss der Fachinformation. Die Salbe wird zweimal täglich (morgens und abends) lokal aufgetragen.
KontraindikationenCrisaborol ist bei einer Überempfindlichkeit kontraindiziert. Die vollständigen Vorsichtsmassnahmen finden sich in der Arzneimittel-Fachinformation.
Unerwünschte WirkungenZu den häufigsten möglichen unerwünschten Wirkungen gehören Schmerzen (ein Brennen und Stechen) an der Applikationsstelle. Über Überempfindlichkeitsreaktionen wurde berichtet.
siehe auchAtopische Dermatitis, Phosphodiesterase-4-Hemmer
Literatur- Arzneimittel-Fachinformation (USA)
- Food and Drug Administration (FDA)
- Murrell D.F., Gebauer K., Spelman L., Zane L.T. Crisaborole Topical Ointment, 2% in Adults With Atopic Dermatitis: A Phase 2a, Vehicle-Controlled, Proof-of-Concept Study. J Drugs Dermatol, 2015, 14(10), 1108-12 Pubmed

- Pfizer.com
- Stein Gold L.F., Spelman L., Spellman M.C., Hughes M.H., Zane L.T. A Phase 2, Randomized, Controlled, Dose-Ranging Study Evaluating Crisaborole Topical Ointment, 0.5% and 2% in Adolescents With Mild to Moderate Atopic Dermatitis. J Drugs Dermatol, 2015, 14(12), 1394-9 Pubmed

- Tom W.L., Van Syoc M., Chanda S., Zane L.T. Pharmacokinetic Profile, Safety, and Tolerability of Crisaborole Topical Ointment, 2% in Adolescents with Atopic Dermatitis: An Open-Label Phase 2a Study. Pediatr Dermatol, 2016 Pubmed

Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.
Weitere InformationenPharmaWiki mit Google durchsuchen.
