Radioaktivität
 PharmaWiki
PharmaWikisynonym: Radioaktiver Zerfall, Radioelemente, Radionuklide, Ionisierende Strahlung
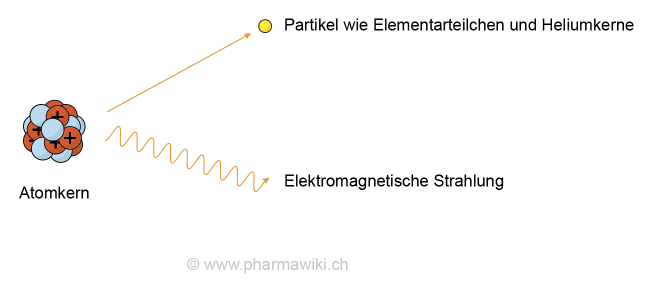
Über die RadioaktivitätDie Radioaktivität ist ein natürliches Phänomen, bei dem Partikel (Teilchenstrahlung) oder elektromagnetische Strahlung aus dem Kern von Atomen freigesetzt werden. Dies wird als ionisierende Strahlung bezeichnet. Sie führt zu einem Energieverlust des Kerns.
Die wichtigsten ionisierenden Strahlen sind die Alphastrahlung, die Betastrahlung (Beta-Minus und Beta-Plus) und die Gammastrahlung:
- Alpha: Heliumkern
- Beta-Minus: Elektron, Antineutrino
- Beta-Plus: Positron (positives Antiteilchen des Elektrons), Neutrino
- Gamma: Kurzwellige elektromagnetische Strahlung
Radioaktivität, zum Vergrössern anklicken. Illustration © PharmaWiki
Weil die Radioaktivität unsichtbar ist, wurde sie erst im Jahr 1896 von französischen Physiker Henri Becquerel beim Studium der Phosphoreszenz entdeckt. Phosphoreszenz bedeutet, dass ein Stoff für einige Zeit leuchtet, nachdem er mit Licht oder UV-Strahlung bestrahlt wurde (Nachleuchten). Die polnisch-französische Physikerin Marie Curie und ihre Ehemann Piere prägten zwei Jahre später den Begriff radioactivité. Sie entdeckten zwei neue radioaktive Elemente, nämlich Radium und Polonium.
Radioaktivität bedeutet, dass die Atomkerne aufgrund eines Ungleichgewichts der Protonen und Neutronen unstabil sind und sich unter der Freisetzung von Energie in andere Kerne umwandeln oder ihren Zustand ändern. Grosse Atomkerne sind dafür besonders anfällig. Die Umwandlung eines Elements in ein anderes wird als Transmutation bezeichnet und war das klassische Ziel der Alchemisten.
Zu den bekanntesten radioaktiven Stoffen gehört das Uranisotop Uran-235, dessen Kern 92 Protonen und 143 Neutronen enthält. Es zerfällt über viele Radioisotope schliesslich zum stabilen Blei-206. Es wird von einer Zerfallsreihe gesprochen. Daran zeigt sich, dass der entstandene Kern radioaktiv sein kann oder nicht.
Weitere bekannte radioaktive Elemente und Isotope:
Isotope eines Elements können sowohl stabil als auch radioaktiv sein. Es gibt nicht ein Element, von dem kein radioaktives Isotop bekannt wäre.
Die Radioaktivität von Atomen ist eine Eigenschaft, die sich mit der Zeit verliert. Viele Radioisotope kommen auf der Erde nicht mehr vor, weil sie seit ihrer Entstehung mittlerweile zerfallen sind. Als Mass wird die Halbwertszeit verwendet, also die Zeitspanne, in welcher die Hälfte der radioaktiven Kerne zerfallen sind. Sie ist sehr unterschiedlich und reicht abhängig vom Radionuklid von Sekunden bis zu Milliarden von Jahren und weit darüber hinaus.
Die Energie der natürlichen Radioelemente stammt aus den Sternen, wo die Nuklide durch Kernfusion entstanden sind.
Wir sind der Radioaktivität täglich ausgesetzt, weil Radioelemente in der Atmosphäre, in der Erdkruste und in unserem Essen vorkommen. Dazu gehören Uran, Radon und Kohlenstoffisotope. Uran kommt beispielsweise im Alpenraum häufig vor. Das radioaktive Isotop Kalium-40 hat eine sehr lange Halbwertszeit und ist Teil des natürlichen Kaliumpools. Des Weiteren werden Radioisotope auch künstlich hergestellt und beispielsweise in der Medizin, der Technik und in der wissenschaftlichen Forschung und Entwicklung verwendet.
Als Mass, wie häufig ein Zerfall stattfindet, wird das Becquerel verwendet (Bq). 1 Bq ist definiert als ein Zerfall in einer Sekunde.
Zu viel Strahlung innert kurzer Zeit ist für die Zellen des menschlichen Körpers toxisch. Sie sterben ab und es entsteht die sogenannte → Strahlenkrankheit. Bei einer zu hohen Dosis ist sie in jedem Fall tödlich.
Radiopharmaka sind Arzneimittel, welche radioaktive Isotope enthalten und für die Diagnose und Therapie von Krankheiten verwendet werden.
siehe auchUran, Strahlenkrankheit, Chemische Elemente, Radiopharmaka
Literatur- Fachliteratur
Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.