Kaliumpermanganat
 Arzneimittelgruppen
Arzneimittelgruppen  Salze
Salze  Oxidationsmittel Kaliumpermanganat ist ein Wirkstoff aus der Gruppe der Oxidationsmittel mit oxidierenden, desinfizierenden, desodorierenden und adstringierenden Eigenschaften. Es wurde unter anderem für Mundspülungen und für die Wundreinigung und -desinfektion verwendet. Heute wird es nur noch selten eingesetzt. Bei der Abgabe muss berücksichtigt werden, dass Kaliumpermanganat für die Herstellung von Explosivstoffen geeignet ist.
Oxidationsmittel Kaliumpermanganat ist ein Wirkstoff aus der Gruppe der Oxidationsmittel mit oxidierenden, desinfizierenden, desodorierenden und adstringierenden Eigenschaften. Es wurde unter anderem für Mundspülungen und für die Wundreinigung und -desinfektion verwendet. Heute wird es nur noch selten eingesetzt. Bei der Abgabe muss berücksichtigt werden, dass Kaliumpermanganat für die Herstellung von Explosivstoffen geeignet ist. synonym: Kalii permanganas PhEur, KMnO4
ProdukteReines Kaliumpermanganat ist als Offenware und abgefüllt in Apotheken und Drogerien erhältlich.
Struktur und EigenschaftenKaliumpermanganat (KMnO4, Mr = 158.0 g/mol) liegt als dunkelviolettes bis bräunlich schwarzes, körniges Pulver oder als dunkelviolette bis fast schwarze, metallisch glänzende Kristalle vor und ist in siedendem Wasser leicht löslich. Die Substanz zersetzt sich beim Kontakt mit verschiedenen organischen Stoffen und mit einigen Stoffen besteht ein Explosionsrisiko (siehe unten). Die Oxidationszahl beträgt für das Mangan +7.
Struktur: K+MnO4-
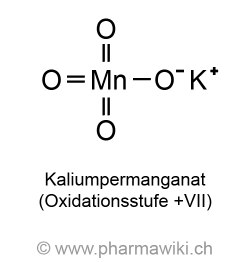
Kaliumpermanganat (ATC D08AX06  , ATC V03AB18
, ATC V03AB18  ) ist ein starkes Oxidationsmittel. Es hat desinfizierende, oxidierende, desodorierende und adstringierende Eigenschaften.
) ist ein starkes Oxidationsmittel. Es hat desinfizierende, oxidierende, desodorierende und adstringierende Eigenschaften.
- Kaliumpermanganat wurde medizinisch in Form einer stark verdünnten Lösung unter anderem zur Wundreinigung und -desinfektion und für für Mundwässer eingesetzt. Heute wird es nur noch selten verwendet.
- Hauterkrankungen, Pilzinfektionen
- Als Reagens, für die organische Synthese
- Als Antidot
- In der Tiermedizin, bei Zierfischen
Für chemische Experimente (Redox-Reaktion): Werden einige Tropfen Glycerol zu Kaliumpermanganat gegeben, kommt es zu einer heftigen exothermen Reaktion mit einer violetten Flamme und einer Funken- und Wärmebildung:
- 14 KMnO4 (Kaliumpermanganat) + 4 C3H8O3 (Glycerol) → 7 K2CO3 (Kaliumcarbonat) + 7 Mn2O3 (Mangan(III)-oxid) + 5 CO2 (Kohlenstoffdioxid) + 16 H2O (Wasser)
Bei der Abgabe muss berücksichtigt werden, dass Kaliumpermanganat zur Herstellung explosiver und brennbarer Verbindungen geeignet ist. Jugendliche färben damit zum Spass auch Brunnen.
siehe auchLiteraturAutorInteressenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.
Weitere InformationenPharmaWiki mit Google durchsuchen.
