Edaravon
 Arzneimittelgruppen
Arzneimittelgruppen  AntioxidantienEdaravon ist ein antioxidativer und neuroprotektiver Wirkstoff aus der Gruppe der Antioxidantien, der für die Behandlung der amyotrophen Lateralsklerose (ALS) eingesetzt wird. In einigen Ländern ist er auch für die Therapie eines akuten ischämischen Schlaganfalls zugelasen. Das Arzneimittel wird als intravenöse Infusion verabreicht. Zu den häufigsten möglichen unerwünschten Wirkungen gehören Prellungen, Gangstörungen und Kopfschmerzen. Edaravon hat ein geringes Interaktionspotential.
AntioxidantienEdaravon ist ein antioxidativer und neuroprotektiver Wirkstoff aus der Gruppe der Antioxidantien, der für die Behandlung der amyotrophen Lateralsklerose (ALS) eingesetzt wird. In einigen Ländern ist er auch für die Therapie eines akuten ischämischen Schlaganfalls zugelasen. Das Arzneimittel wird als intravenöse Infusion verabreicht. Zu den häufigsten möglichen unerwünschten Wirkungen gehören Prellungen, Gangstörungen und Kopfschmerzen. Edaravon hat ein geringes Interaktionspotential.synonym: Edaravonum, MCI-186
ProdukteFür die ALS-Behandlung wurde Edaravon in Japan im Jahr 2015 und in den USA im Jahr 2017 als Infusionspräparat zugelassen (Radicava®). In der Schweiz ist das Arzneimittel seit dem Jahr 2019 registriert. Im Jahr 2023 wurde eine Suspension zum Einnehmen freigegeben.
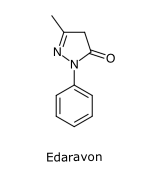
Struktur und EigenschaftenEdaravon (C10H10N2O, Mr = 174.2 g/mol) ist ein substituiertes 2-Pyrazolin-5-on. Es liegt als weisses, kristallines Pulver vor, das in Wasser nur wenig löslich ist.
Edaravon (ATC N07XX14  ) ist ein Radikalfänger mit antioxidativen und neuroprotektiven Eigenschaften. Es reduziert den oxidativen Stress und verlangsamt den Krankheitsverlauf. Die Halbwertszeit liegt zwischen 4.5 bis 6 Stunden.
) ist ein Radikalfänger mit antioxidativen und neuroprotektiven Eigenschaften. Es reduziert den oxidativen Stress und verlangsamt den Krankheitsverlauf. Die Halbwertszeit liegt zwischen 4.5 bis 6 Stunden.
Für die Behandlung der amyotrophen Lateralsklerose (ALS).
In Japan zusätzlich für die Behandlung eines akuten ischämischen Schlaganfalls (Zulassung 2001). Dieser Artikel bezieht sich auf die ALS.
DosierungGemäss der Fachinformation.
Kontraindikationen- Überempfindlichkeit
- Schwangerschaft
Die vollständigen Vorsichtsmassnahmen finden sich in der Arzneimittel-Fachinformation.
InteraktionenEdaravon wird sulfatiert und konjugiert. Es ist ein Substrat von Glucuronsyltransferasen (UGT) und Sulfotransferasen. Es interagiert nicht mit CYP450-Isoenzymen.
Unerwünschte WirkungenZu den häufigsten möglichen unerwünschten Wirkungen gehören Prellungen, Gangstörungen und Kopfschmerzen.
siehe auchLiteratur- Abe K. et al. Confirmatory double-blind, parallel-group, placebo-controlled study of efficacy and safety of edaravone (MCI-186) in amyotrophic lateral sclerosis patients. Amyotroph Lateral Scler Frontotemporal Degener, 2014, 15(7-8), 610-7 Pubmed

- Arzneimittel-Fachinformation (USA)
- EMA
- Feng S. et al. Edaravone for acute ischaemic stroke. Cochrane Database Syst Rev, 2011, CD007230 Pubmed

- FDA
- Herstellerinformationen
- Kikuchi K. et al. The efficacy of edaravone (radicut), a free radical scavenger, for cardiovascular disease. Int J Mol Sci, 2013, 14(7), 13909-30 Pubmed

Interessenkonflikte: Keine / unabhängig. Der Autor hat keine Beziehungen zu den Herstellern und ist nicht am Verkauf der erwähnten Produkte beteiligt.
Weitere InformationenWirkstoffe: Edaravonum
Unternehmen: Mitsubishi Tanabe Pharma GmbH, Düsseldorf, Zweigniederlassung Lenzburg
Abgabekategorie: B
Gruppe / Anwendung: Andere ZNS-Mittel
Wirkstoffe: Edaravonum
Unternehmen: Mitsubishi Tanabe Pharma GmbH, Düsseldorf, Zweigniederlassung Lenzburg
Abgabekategorie: B
Gruppe / Anwendung: Andere ZNS-Mittel
